
炭素イオンの基礎知識
炭素1コのイオンは自然界では通常存在しません。
炭素はL殻の電子数が4個で安定していているため「電子の授受が起きない=イオン化しない」と考えられています。
有機化学ではカルボカチオン(炭素原子上に正電荷をもつ)が、反応の中間体として出てくることがあります。
しかし、これは高校化学の範囲を超えているので、特別に覚える必要はありません。
炭素のイオン式(化学式)
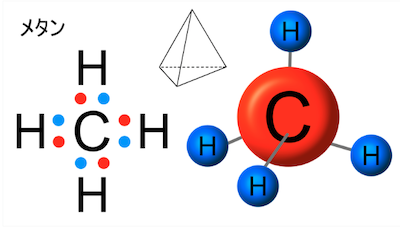
炭素は通常、イオンを形成することは少ないです。これは、炭素が外殻に4つの電子を持っており、8つの電子を持つ安定な状態になるためには4つの電子を取得するか、4つの電子を放出する必要があるためです。
このような大きな電子の授受はエネルギー的に不利であるため、炭素は通常、共有結合を形成します。
ただし、特定の反応条件下で炭素イオンが形成されることがあります。
以下は炭素イオンとして最も一般的に知られているイオン式の例です:
- カルボカチオン: 炭素が正の電荷を持つカチオン。例: CH3+
- カルボアニオン: 炭素が負の電荷を持つアニオン。例: CH3−
これらのイオンは、特定の有機化学反応の中間体として一時的に形成されることがあります。
炭素がイオンを形成することは稀であり、その存在は主に有機化学の反応の文脈で議論されます。
炭素イオンのQ&A
炭素は何価のイオン?
炭素は四価の元素です。
これは、炭素の原子が外殻に4つの電子を持っているため、4つの共有結合を形成する能力を持っていることを意味します。
炭素イオンビームとは?
炭素イオンビームは、炭素イオンを高速で加速し、特定のターゲットに向けて放射するビームのことを指します。
この技術は、特に医療分野でのがん治療において注目されています。炭素イオンビームは、X線やガンマ線に比べて、がん細胞に対する破壊力が高く、周囲の正常な組織への影響が少ないという特徴があります。
このため、炭素イオンビームを使用した放射線治療(炭素イオン線治療)は、特に深部のがんや放射線治療が難しいがんに対して効果的であるとされています。
炭素のイオン化傾向は?
炭素は周期表の第14族に位置しており、その電子配置は1s^2 2s^2 2p^2です。
この配置により、炭素は4つの共有結合を形成する傾向があります。炭素は通常、4つの電子を共有して八重項則を満たすため、イオンを形成することは少ないです。
しかし、特定の条件下で、炭素はC^4+またはC^4-のイオンを形成することができます。C^4-のイオンはカーバイドイオンとして知られています。
炭素の第一イオン化エネルギーは、炭素が他の原子と結合する際のエネルギーの変化を示しています。炭素がイオンを形成する傾向は低いため、そのイオン化エネルギーは比較的高いです。
炭素の化学的性質や反応性は、そのイオン化傾向や共有結合の形成能力に大きく影響されます。炭素は生命の基盤となる多くの有機化合物を形成する能力を持っており、その多様性は炭素の化学的性質に起因しています。
以上です。